El fruto de sabal mejora los síntomas de la hiperplasia benigna de próstata y la disfunción sexual. resultados de un estudio piloto. revista de fitoterapia 2012; 12 (2): 119-133.
Volumen 12, N.º 2 · Diciembre 2012
Separata de la Revista de Fitoterapia 2012; 12 (2): 119-133
Revista de
El fruto de sabal
mejora los síntomas
de la hiperplasia
benigna de próstata y
la disfunción sexual.
Resultados de un
Andreas Suter Reinhard Saller Eugen Riedi Michael Heinrich
Edición especial para
Revista de Fitoterapia 2012; 12 (2): 119-133
FIGURA 1. Fruto de sabal (
Serenoa repens). Foto: Steven Foster.
El fruto de sabal mejora los síntomas de la
hiperplasia benigna de próstata y la disfunción
sexual. Resultados de un estudio piloto
Andreas Suter a, d
Reinhard Saller b
La hiperplasia prostática benigna (HPB) es un importante factor de
riesgo para la disfunción sexual. Además, el tratamiento estándar, los
bloqueadores α-adrenérgicos y los inhibidores de la 5α-reductasa,
Michael Heinrich d
pueden causar a su vez disfunción sexual. Los preparados del fruto
de sabal (
Serenoa repens (W. Bartram) Small)
son un tratamiento efi-
a Departamento médico, A. Vogel
caz y bien tolerado para la HPB leve o moderada y se han utilizado
Bioforce AG, Roggwil, Suiza
tradicionalmente para tratar disfunciones sexuales. Se ha llevado a
b Instituto de Medicina Natural, Zurich
cabo un estudio clínico piloto, abierto, multicéntrico para investigar si
University Hospital, Zurich, Suiza
el preparado de fruto de sabal
Prostasan® (comercializado en España
como Sabalsan®) influye en los síntomas de la HPB y las disfuncio-
Consulta Urológica, Chur, Suiza
nes sexuales. Ochenta y dos pacientes participaron en el estudio, de
d Escuela de Farmacia, University of
8 semanas de duración, tomando una cápsula diaria (320 mg) de un
London, University College London,
extracto lipofílico de fruto de sabal. Al final del tratamiento, la pun-
Londres, Reino Unido
tuación en la escala internacional de síntomas prostáticos (IPSS) se
redujo de 14,4 a 6,9 (
p <0,0001); las disfunciones sexuales, medidas
Dirección de contacto:
con el inventario breve de la función sexual mejoraron de 22,4 a 31,4
(
p <0,0001); la puntuación del componente de la vida sexual del cues-
A. Vogel Bioforce AG
tionario de calidad de vida para la HPB (Urolife BPH QoL-9 sex), mejoró
de 137,3 a 195 (
p <0,0001). Las evaluaciones de los investigadores y
CH-9325 Roggwil, Suiza
pacientes confirmaron la eficacia, tolerabilidad y aceptación por los
pacientes. Los análisis de correlación confirmaron la vinculación entre
la mejoría de los síntomas de la HPB y la reducción de la disfunción se-
xual. Este es el primer estudio que demuestra una mejoría simultánea
en los síntomas de la HPB y las disfunciones sexuales con extracto de
fruto de sabal.
Palabras clave
Hiperplasia prostática benigna, disfunciones sexuales, ensayo clínico,
Sabal,
Serenoa repens, Sabal serrulata.
Cita Publicaciones
Revista de Fitoterapia 2012; 12 (2): 119-133
O fruto de Palmeto melhora os sintomas da hi-
Saw palmetto berry improves BPH symptoms
perplasia benigna da próstata e a disfunção
and sexual dysfunctions. Results from a pilot
sexual. Resultados de um estudo piloto
A hiperplasia benigna da próstata (HBP) é um importante
The benign prostate hyperplasia (BPH) is a major risk
fator de risco para a disfunção sexual. Além disso, o trata-
factor for sexual dysfunctions. Additionally, the stan-
mento usual com bloqueadores α-adrenérgicos e inibido-
dard treatments for BPH symptoms, alpha-blockers and
res da 5α-reductase podem causar disfunção sexual. Pre-
5α-reductase inhibitors, cause sexual dysfunctions them-
parações à base de fruto de palmeto (
Serenoa repens (W.
selves. Preparations from saw palmetto (
Serenoa repens
Bartram) Small) são um tratamento eficaz e bem tolerado
(W. Bartram) Small) fruit have shown efficacy and good
para a HBP ligeira a moderada e têm sido tradicionalmente
tolerability in the treatment for mild or moderate BPH and
usadas para tratar a disfunção sexual. Foi realizado um es-
have traditionally been used to treat sexual dysfunctions.
tudo clínico piloto, multicêntrico, aberto para investigar se
We conducted an open, multicentric, clinical pilot trial to
o preparado do fruto de palmeto Prostasan® (comercializa-
investigate whether ProstasanTM (marketed in Spain as
do em Espanha como Sabalsan®) influencia os sintomas da
SabalsanTM), a preparation of saw palmetto fruit, influ-
HBP e a disfunção sexual. 82 doentes participaram no es-
enced BPH symptoms and sexual dysfunctions. Eighty two
tudo por oito semanas, tomando uma cápsula por dia (320
patients participated in a 8-week trial, taking one capsule
mg) de extrato lipofílico de fruto de palmeto. Após o trata-
(320 mg) of the saw palmetto lipophilic extract daily. At the
mento, a pontuação no índice internacional de sintomas
end of the treatment, the International Prostate Symptom
prostáticos (IPSS) diminuiu de14,4 para 6,9 (p <0,0001); a
Score (IPSS) was reduced from 14.4 to 6.9 (p < 0.0001).
disfunção sexual, medida por um questionário breve da
Sexual dysfunctions measured with the brief Sexual Func-
função sexual melhorou de 22,4 para 31,4 (p <0,0001), a
tion Inventory improved from 22.4 to 31.4 (p < 0.0001),
pontuação do inquérito relativo ao componente sexual do
and the score of the component regarding sexual life of
questionário da qualidade de vida para a HBP (Urolife BPH
the life quality questionnaire for benign prostatic hyper-
QV-9), melhorou de 137,3 para 195 (p <0,0001). As ava-
plasia (Urolife BPH QoL-9 sex) improved from 137,3 to
liações dos investigadores e doentes confirmaram a efi-
195 (p < 0.0001). Investigators' and patients' assessments
cácia, tolerabilidade e aceitação do paciente. As análises
confirmed the efficacy, tolerability and acceptance by the
de correlação confirmaram a ligação entre a melhoria dos
patients. Correlation analyses confirmed the relationship
sintomas da HBP e a redução da disfunção sexual. Este é
between improved BPH symptoms and reduced sexual dys-
o primeiro estudo a demonstrar uma melhoria simultânea
functions. This is the first trial with
Sabal serrulata show-
nos sintomas da HBP e na disfunção sexual com um extrac-
ing improvement in BPH symptoms and in sexual dysfunc-
to do fruto de palmeto.
tion as well.
Hiperplasia benigna da prostata, disfunção sexual, ensaio
Benign prostate hyperplasia, sexual dysfunctions, clinical
clínico, Palmeto,
Serenoa repens, Sabal serrulata.
trial, saw palmetto,
Serenoa repens, Sabal serrulata.
y en la mitad de los hombres mayores de 80 (3), aunque la
La próstata es un órgano glandular fibromuscular que se en-
presencia histológica de la HPB se observa en más del 90%
cuentra situado entre la vejiga urinaria y el suelo pélvico y
de los hombres en este último grupo de edad (4).
rodea la uretra (1). A partir de los 40 años, puede proliferar
Aparte de los síntomas obstructivos e irritativos (TABLA
dando lugar a un crecimiento, no maligno, que se conoce
1), la HPB también influye negativamente en las funciones
como hiperplasia próstática benigna (HPB) (2) y que conduce a
sexuales (5). Los estudios epidemiológicos muestran que,
la constricción de la uretra. Ésta da lugar a síntomas del trac-
junto con el proceso de envejecimiento en general, los sín-
to urinario inferior (STUI), como un aumento en la frecuencia
tomas urinarios asociados a la HPB son un factor clave en
urinaria, urgencia miccional, nicturia, vaciamiento incomple-
el desarrollo de la disfunción eréctil y los trastornos de la
to de la vejiga y chorro de orina débil. Estos síntomas se
eyaculación (6, 7), representando un factor de riesgo mayor
manifiestan en cerca de un tercio de los hombres de 60 años
que la diabetes, la hipertensión, las enfermedades car-
Cita Publicaciones
Revista de Fitoterapia 2012; 12 (2): 119-133
diacas, o las hiperlipidemias (7). En general parece existir una asociación clara y clínicamente significativa entre los síntomas urinarios asociados del tracto urinario inferior y varios tipos de disfunciones sexuales en hombres de edad avanzada en todo el mundo. A partir de datos epidemioló-gicos, Rosen
et al. (8) llegaron a la conclusión de que, en comparación con los pacientes asintomáticos, los pacien-tes con HPB tenían un riesgo 3,7 veces mayor de desarro-llar disfunción eréctil durante los dos años posteriores a la aparición de los síntomas de la HPB. Además, la severidad de los STUI se correlacionó con la aparición más frecuente y más grave de disfunción eréctil y eyaculatoria (8).
Los principales tratamientos médicos para los síntomas de la HPB incluyen bloqueadores α-adrenérgicos como la tamsulosina, doxazosina y alfuzosina (9), que proporcio-nan un rápido alivio de los STUI (10) o los inhibidores de la 5α-reductasa como finasterida o dutasterida, que pro-porcionan un alivio de los síntomas tras 6-9 meses y son más útiles en pacientes con próstatas de gran tamaño (11). Ambas opciones de tratamiento presentan efectos benefi-ciosos sobre los síntomas de la HPB, sin embargo tienen un impacto negativo significativo en la función sexual. La principal disfunción sexual reportada en la terapia con blo-
FIGURA 2. Flujo urinario en el aparato genitourinario masculino nor-
queadores α-adrenérgicos es la eyaculación retrógrada o
mal (arriba) y con hiperplasia benigna de próstata (abajo). Imagen
anormal, lo que ocurre en el 4-18% de los pacientes tra-
tados con tamsulosina, incrementándose hasta el 30% en
cada por: Josep Vanaclocha.
su uso a largo plazo (12). Los estudios sobre los inhibidores
Obstructivos o de vaciado
de la 5α-reductasa reportan disfunciones sexuales con una
Vaciado incompleto
frecuencia del 2,1% al 38%, siendo la más importante la
Micción intermitente
disfunción eréctil, seguido de la disminución de la libido y
Menor calibre y fuerza del chorro de orina
trastornos de la eyaculación (13). Las disfunciones sexuales
son las reacciones adversas reportadas con mayor frecuen-cia en caso de los inhibidores de la 5α-reductasa, descritas
Irritativos o de llenado
en proporciones similares para finasterida y dutasterida (14).
Urgencia miccional
Los preparados a base de fruto de sabal,
Serenoa repens
(W. Bartram) Small (sinónimo
Sabal serrulata (Michx.)
Schult.f.) (FIGURA 1) han sido utilizados tradicionalmente
Pesadez y dolor suprapúbico
para el tratamiento de los síntomas leves a moderados de la HPB. La planta, originaria de Florida (EUA), fue utiliza-da por primera vez por los colonos blancos en los Estados
TABLA 1. Síntomas del tracto urinario inferior asociados a la HPB.
Unidos para el tratamiento de los STUI, y curiosamente
Las manifestaciones de vaciado se deben a la obstrucción mecá-
también como tratamiento para la disfunción eréctil, para
nica ejercida sobre el cuello vesical por el agrandamiento de la próstata; las irritativas están relacionadas con la inestabilidad del
mejorar la atrofia testicular y la producción de esperma, así
músculo detrusor y la disfunción vesical.
como estimulante sexual (15). Se han realizado más de 30
Cita Publicaciones
Revista de Fitoterapia 2012; 12 (2): 119-133
estudios clínicos controlados para investigar el tratamien-
Criterios de inclusión
to de la HPB con preparados de sabal, que por lo general consisten en un extracto lipofílico de los frutos, en dosis de
Pacientes de sexo masculino entre 18-80 años de edad con
320 mg diarios (16). En comparación con el placebo, los estu-
una puntuación en la escala IPSS > 7
dios demuestran una buena eficacia a largo plazo del estos
Presencia de síntomas de HPB durante al menos dos meses
preparados para tratar los síntomas de la HPB. En general
Disfunción sexual (disfunción eréctil y/o disminución de la
los resultados son similares a los obtenidos con finasterida
libido) durante al menos dos meses
(17) y tamsulosina (18), pero el fruto de sabal tiene un perfil de
Deseo sexual: puntuación < 5 en el inventario breve de la
seguridad mucho mejor que el de estas sustancias, en par-
función sexual (bSFI)
ticular en lo que respecta a las disfunciones sexuales (19).
Deseo y posibilidad de actividad sexual (masturbación, pare-
Se han reportado como modos de acción,
in vitro e
in vivo,
ja sexual), sin trastornos orgánicos que impidan la práctica
la inhibición de las dos isoformas de la 5α-reductasa (20, 21),
sexual (impedimento físico o vascular, etc.)
actividades antiinflamatorias (22, 23), así como la inhibición
Disposición a contestar con sinceridad las preguntas sobre
de los receptores autónomos del tracto urinario inferior (24).
Sería deseable disponer de un tratamiento que mejore los
Consentimiento informado por escrito del paciente
síntomas de la HPB sin afectar negativamente las funcio-
Criterios de exclusión
nes sexuales y, si es posible, que incluso tenga un impacto positivo sobre ellas (25). Con este objetivo, se llevó a cabo
Falta de libido debido a una enfermedad psiquiátrica o a un
un estudio clínico piloto para investigar si un extracto es-
estado de ánimo depresivo
tandarizado de fruto de sabal incidía en las disfunciones
Falta de libido en los dos últimos meses, según evaluación
sexuales en pacientes con HPB leve a moderada.
del investigadorPacientes con trastornos vasculares graves (microangiopa-
Pacientes y métodos
tía) o diabetes mellitus severa
Pacientes con hipertensión estable en tratamiento con un medicamento antihipertensivo durante menos de dos meses
El estudio se llevó a cabo entre junio de 2009 y octubre
Neuropatías conocidas
de 2010 en dos consultas urológicas y cuatro de medici-na general de Suiza, en pacientes con síntomas al menos
Predisposición poco favorable del paciente
moderados de HPB y disfunciones sexuales, tales como
Participación en algún ensayo clínico en los últimos 2 meses
disfunción eréctil o falta de deseo sexual. El estudio fue
previos al estudio
aprobado por los correspondientes comités éticos canto-
Consumo de alcohol o abuso de drogas
nales y se llevó a cabo de conformidad con las normas de
Cirugía programada durante el período de observación
buenas prácticas clínicas y las obligaciones éticas de la Declaración de Helsinki. La autoridad reguladora suiza, Swissmedic, notificó el estudio que está inscrito en el re-
TABLA 2. Criterios de inclusión y exclusión en el estudio. IPSS: Puntuación en la escala internacional de los síntomas prostáticos.
gistro internacional de estudios clínicos ClinicalTrials.gov,
bSFI: inventario breve de la función sexual.
con número identificador NCT01021267. Los criterios de inclusión y exclusión se muestran en la TABLA 2.
A los participantes se les prohibió la toma regular (más
Medicación ensayada y desarrollo del estudio
de 1 unidad cada 2 semanas) de inhibidores de la fosfo-
Se realizó un estudio clínico abierto con una duración to-
diesterasa-5 (PDE-5) y su ingesta en los 4 días anteriores
tal de nueve semanas por paciente, que consistió en una
al inicio del estudio. Si no se habían tomado de manera
semana previa (periodo de rodaje) para observar si los
continua durante 3 meses como tratamiento estable, tam-
síntomas de la HPB y disfunciones sexuales se mantenían
poco fueron permitidos los medicamentos concomitantes
estables y posteriormente un periodo de tratamiento de 8
siguientes: inhibidores de la 5α-reductasa, alfa antago-
semanas. En cada visita se registraron los parámetros de
nistas, AINEs (de síntesis o fitoterápicos), paracetamol, y
eficacia. El medicamento de prueba consistió en 320 mg/
agentes antidepresivos de síntesis.
día (una cápsula) de un extracto lipofílico de fruto de sa-
Cita Publicaciones
Revista de Fitoterapia 2012; 12 (2): 119-133
bal, con una relación droga: extracto de 9-12:1, (disolven-
corregida y luego utilizada por un médico de habla alema-
te: etanol 96% V/V), fabricado por A. Vogel Bioforce AG,
na en su práctica diaria. Basándose en sus experiencias,
Roggwil, Suiza (Prostasan®, lote 025070 NR). El fruto de
se hicieron nuevas correcciones y así se completaron las
sabal utilizado procedía de cultivo orgánico certificado pro-
versiones finales alemanas. Al final del tratamiento, la
pio de A. Vogel Bioforce en Florida, EEUU) y cumplía con las
evaluación global de la eficacia por el paciente y el inves-
disposiciones de la Farmacopea Europea. Una cápsula de
tigador se realizó en una escala de 4 puntos (muy buena,
este lote contenía 275 mg de ácidos grasos, que compren-
buena, regular o mala).
dían 29,5% de ácido láurico, 39,2% de ácido oleico y lino-
Los parámetros de seguridad incluían la aparición de reac-
leico, 13,5% de ácido mirístico y 10% de ácido palmítico.
ciones adversas y la evaluación global de la seguridad por
En la segunda visita, cada paciente recibió un frasco con
parte de los pacientes y los investigadores, al final del tra-
90 cápsulas y el cumplimiento del protocolo se comprobó
tamiento, calificándola como muy buena, buena, regular o
contando los comprimidos restantes en la última visita del
Además, se hicieron preguntas acerca de las rutinas dia-
Los cambios en los síntomas de la HPB se evaluaron utili-
rias de los pacientes. A los pacientes se les preguntó si
zando el IPSS, las disfunciones sexuales con el bSFI y con
estarían dispuestos a seguir tomando el medicamento, lo
el componente sobre la vida sexual del cuestionario de ca-
importante que era para ellos utilizar un tratamiento a base
lidad de vida para la HPB (Urolife BPH QoL-9 sex).
de plantas, y si preferían un medicamento fitoterápico en lugar de la medicación de síntesis. A los investigadores
El formulario IPSS evalúa los síntomas del tracto urina-
se les preguntó si utilizarían de nuevo el medicamento del
rio bajo. La puntuación se calcula mediante la respuesta
estudio y si contestaban afirmativamente se les pedía ex-
del paciente a preguntas referidas a su propia experien-
poner sus razones para ello.
cia; cuanto más alta es la puntuación, más severa es la afectación. Como el cálculo se basa en las respuestas del
Análisis estadístico
paciente, es un buen método de estimación del efecto de
Como se trataba de un estudio clínico abierto, se utilizó
los síntomas urinarios en la calidad de vida de la persona.
estadística descriptiva utilizando los programas Excel (Mi-
El bSFI es un cuestionario en el que el paciente auto-evalúa
crosoft Corporation, Redmond, Washington, EE.UU.) y SAS,
su sexualidad tanto en la dimensión fisiológica de la exci-
versión 9.2 (SAS Institute, Enhanced Logging Facilities,
tación y del orgasmo, como la psicológica del deseo y la
Cary, NC, USA.). Las comparaciones de los cambios dentro
satisfacción sexual, con dos preguntas sobre el deseo se-
del grupo de determinaciones del IPSS, bSFI y Urolife BPH
xual, tres sobre erecciones, dos sobre eyaculación, cuatro
QoL 9 sex entre la visita 1 y la visita 2 y entre la visita 2 y
sobre la evaluación de problemas y una pregunta sobre la
la visita 3 se llevó a cabo utilizando el test Wilcoxon para
satisfacción general. Cada pregunta se evalúa en una es-
las diferencias pareadas.
cala de 0 (mayor gravedad del problema) a 4 (ausencia de
Las correlaciones entre los cambios del IPSS y el bSFI, del
problema) (26). El Urolife BPH QoL-9 es un cuestionario vali-
IPSS y el Urolife BPH QoL 9 sex y del bSFI Urolife BPH QoL
dado de 9 preguntas, tres de las cuales hacen referencia a
9 sex, fueron analizadas por el cálculo del coeficiente de
la percepción de los pacientes sobre su vida sexual: deseo,
correlación de Pearson.
erección y satisfacción sexual; cada pregunta se evalúa en
una escala visual analógica de 100 mm, que va desde 0 (sin satisfacción) a 100 (máxima satisfacción) (27). Se utili-
zaron los dos cuestionarios para poder apreciar mejor los
Se reclutaron un total de 82 pacientes, conformando la po-
cambios en las disfunciones sexuales. Dado que no existía
blación por intención de tratar. Trece pacientes tuvieron al
una versión validada en alemán de los cuestionarios, se
menos una desviación importante y fueron excluidos de la
tradujo por primera vez al alemán por dos traductores in-
población por protocolo, que fue utilizada para el análisis
dependientes. A partir de estas dos versiones traducidas,
se hizo una versión compilada en alemán, que luego fue
La población por protocolo, o de casos válidos, incluye úni-
re-traducida al inglés por otros dos traductores, para ser
camente a los pacientes que han completado el estudio,
comparada con la versión original. La versión alemana fue
de los que se dispone de todos los datos previstos y en
Cita Publicaciones
Revista de Fitoterapia 2012; 12 (2): 119-133
los que no se han observado irregularidades o violaciones
ción) y cuatro casos de pacientes que no se presentaron a
las visitas de seguimiento. Los pacientes tenían una media
La población por intención de tratar respeta la asignación
de 57,3 ± 11,1 años de edad (TABLA 3).
aleatoria y se atribuyen al tratamiento todos los aconteci-
Un centro reclutó a la mayoría de los pacientes (n = 54), y
mientos ocurridos después de la aleatorización, indepen-
los otros cinco centros a los 15 pacientes restantes. Las
dientemente de cuando hayan ocurrido o de cual haya sido
características basales de los pacientes de este centro
el tratamiento seguido. Proporciona una estimación del
no difirieron significativamente de las de los otros cen-
efecto de cada uno de los tratamientos más cercana a lo
tros. El cumplimiento del período de tratamiento se valoró
que presumiblemente ocurriría en la práctica clínica, donde
como bueno cuando la toma de la medicación fue de un
también existen errores de diagnóstico o incumplimiento
80-120%; el 78,6% de los pacientes cumplieron con este
terapéutico. Sin embargo, la población por protocolo se
criterio, sólo el 7,1% de los pacientes tomó menos del 80%
acerca más al efecto del tratamiento en las condiciones
de la medicación.
óptimas de uso. Si con ambos tipos de población se llega a las mismas conclusiones, se puede considerar que los
resultados del ensayo son más fiables. (28)
No hubo diferencias significativas en ninguno de los pa-
Las desviaciones incluyeron un paciente con IPSS < 7 en
rámetros entre la población por intención de tratar y la
el momento de la inclusión, uno con el componente se-
población por protocolo, por lo tanto, se mostrarán los
xual del bSFI > 5 en el momento de la inclusión, cuatro
resultados de la población por protocolo. Tampoco hubo
pacientes con medicación concomitante no permitida y
cambios estadísticos en los parámetros de eficacia duran-
siete pacientes que no regresaron a la consulta después
te el período de tiempo sin tratamiento (entre la primera y
de la primera visita. Las razones para la interrupción del
segunda visita), pudiéndose observar que los síntomas se
tratamiento incluyen la muerte de la esposa de uno de los
mantuvieron estables y no se alteraron en un corto período
pacientes, dos reacciones adversas (náusea que se evaluó
de tiempo, por lo que se presentarán sólo los resultados de
como relacionada con la medicación del estudio y un ata-
la segunda visita (inicio del tratamiento) y la tercera visita
que isquémico transitorio, no relacionado con la medica-
(final de tratamiento).
Número de pacientes
Edad (media ± DS)
57,3 ± 11,1 años
Peso corporal (media ± DS)
Presión arterial sistólica (media ± DS)
132,5 ± 14,8 mm Hg
Presión arterial diastólica (media ± DS)
84,3 ± 8,3 mm Hg
Frecuencia cardíaca (media ± DS)
Distribución por edad (N):31-40 años
TABLA 3. Características demográficas básicas de la población por protocolo (n = 69). DS: desviación estándar, lpm: latidos por minuto.
Cita Publicaciones
Revista de Fitoterapia 2012; 12 (2): 119-133
- Escala internacional de los síntomas prostáticos (IPSS)
La puntuación en la IPSS se redujo en un 51%, pasando de
14,4 ± 4,7 a 6,9 ± 5,2, después de 8 semanas de tratamien-
to (
p <0,0001). Una puntuación de los síntomas de HPB de
0 a 7 se define como leve, de 8 a 19, moderada y de 20 a
35 como grave. Al inicio del tratamiento, el 18,8% de los
pacientes tenían síntomas graves y 78,3% tenían síntomas
moderados, en la visita final, esto cambió a síntomas leves
en un 63,8% de los pacientes, 31,9% síntomas modera-
dos y sólo un 4,3% con síntomas severos (FIGURA 3). En
cuanto a los elementos individuales que contribuyen a la
puntuación, todos mejoraron significativamente en la mis-
ma medida. El promedio de puntuación de la nicturia pasó
de 1,7 ± 1,1 a 1,0 ± 0,8, la puntuación de la obstrucción de
FIGURA 3. Cambio de la puntuación en la escala IPSS y variación
8,1 ± 3,9 a 3,7 ± 3,7, y la puntuación de la sintomatología
de la intensidad de los síntomas entre el inicio y el final del trata-
irritativa de 6,3 ± 2,6 a 3,2 ± 2,3.
miento (población por protocolo, n = 69,
p < 0,0001).
- Inventario breve de la función sexual (bSFI)La puntuación total del bSFI mejoró de 22,4 ± 7,2 a 31,4 ±
9,2 (
p <0,0001) (FIGURA 4). Las puntuaciones de los compo-
nentes individuales: deseo sexual, función eréctil, función
eyaculatoria, evaluación de problemas y la satisfacción
sexual, mejoraron de forma significativa (
p <0,0001) (TA-
BLA 4 y FIGURA 6). Las mayores mejorías relativas en las
preguntas individuales se observaron en el ámbito de la
evaluación de problemas, donde conseguir y mantener una
erección mejoró en un 64%, tener problemas con la falta
de deseo sexual y eyaculación mejoró cada uno de ellos en
un 54%. Sentir deseo sexual en los últimos 30 días mejoró
en un 47%, y tener una erección lo suficientemente firme
como para tener relaciones sexuales mejoró en un 42%, lo
FIGURA 4. Mejora en el inventario bSFI al inicio y al final del trata-
que, en valores absolutos, es un cambio desde "con bas-
miento (población por protocolo, n = 69,
p <0,0001).
tante frecuencia" a "normalmente".
Hubo un efecto dependiente del centro donde se llevo a
cabo el reclutamiento, mientras que los valores medios
del centro, con la mayoría de los pacientes, mostraron una
mejora significativa, los otros 15 pacientes, agrupados y
reclutados en los otros centros, mostraron solamente una
tendencia (
p = 0,12). De estos quince pacientes, ocho obser-
varon una mejoría, cuatro no observaron cambios y tres un
empeoramiento de su estado, mientras que la gran mayoría
de los pacientes del centro mayoritario, experimentaron al
menos una cierta mejoría de sus disfunciones sexuales.
- Componente de la vida sexual del cuestionario de
calidad de vida para la HPB (Urolife BPH QoL-9 sex)
Se produjo una mejoría en la puntuación del componen-
FIGURA 5. Mejora de la percepción del componente de la calidad
te de la vida sexual del cuestionario Urolife BPH QoL-9
de vida sexual (Urolife QoL-9) entre el inicio y el final de la terapia
de 137,3 ± 47,9 a 195,0 ± 56,3 (p <0,0001) (FIGURA 5).
(población por protocolo, n = 69,
p < 0,0001).
Cita Publicaciones
Revista de Fitoterapia 2012; 12 (2): 119-133
Contrariamente al bSFI, las mejoras en la calidad de vida sexual fueron significativas en todos los centros. Los tres componentes individuales de este cuestionario mejoraron también significativamente como se detalla en la TABLA 4.
- Evaluaciones realizadas por los investigadores y los pacientesLa mayoría de los pacientes calificaron la eficacia como muy buena (22%) o buena (54%) y sólo el 15% vio un pe-queño efecto. Los investigadores evaluaron la eficacia más favorablemente, reportando ser muy buena en un 38% de los casos, buena 44% y sólo el 7% de los pacientes perma-neció sin cambios. Cuando se les preguntó cual de los pa-rámetros de la medicación del estudio tuvo el mejor efecto, el 8% de los pacientes indicó la función eréctil, la libido el
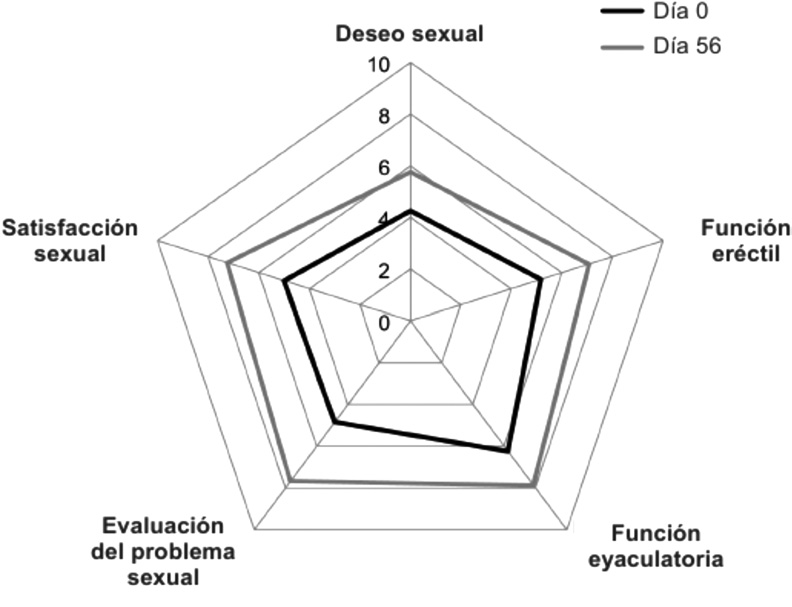
FIGURA 6. Puntuaciones de cada componente del inventario bre-
26% y el 66% la función eréctil y la libido conjuntamente.
ve de la función sexual (bSFI) al inicio y al final del tratamiento, normalizado a una escala de 0-10 (0 = peor, 10 = mejor) (n = 69).
Del total de 82 pacientes, 62 pacientes tomarían las cáp-sulas de nuevo (faltan los datos de seis pacientes) y, en el 91% de los casos, los investigadores utilizarían la me-
de los casos, seguida de la eficacia observada en el 93%
dicación de nuevo. Para el 61% de los pacientes era muy
de los pacientes.
importante que la medicación fuera de origen vegetal y el
- El análisis de correlación
97% de ellos, en caso de la misma eficacia y seguridad,
Se realizaron análisis de correlación para evaluar si los
preferirían los medicamentos fitoterápicos a los de sínte-
cambios en el IPSS, bSFI y el componente de la vida sexual
sis. Los investigadores afirmaron que la razón más impor-
del Urolife BPH QoL-9 estaban asociados. Hubo una corre-
tante para aplicar esta medicación a base de extracto de
lación negativa entre los cambios en el IPSS y el bSFI (ρ
fruto de sabal fue la buena seguridad observada en el 95%
de Pearson = -0,366; p = 0,002) y una correlación negativa
Puntuación de cada componente (mínimo-máximo)
Deseo sexual (0-8)
Función eréctil (0-12)
Función eyaculatoria ( 0-8)
Evaluación de problemas sexuales (0-16)
Satisfacción sexual (0-4)
Urolife BPH QoL-9 sex
Deseo sexual (0-100)
Erecciones (0-100)
Satisfacción sexual (0-100)
TABLA 4. Puntuaciones al inicio (día 0) y final del tratamiento (día 56) de cada componente del bSFI y del Urolife QoL-9 sex. HPB: Hiperplasia Benigna de Prostata. bSFI: Inventario breve de la función sexual. * Test de Wilcoxon.
Cita Publicaciones
Revista de Fitoterapia 2012; 12 (2): 119-133
entre los cambios en el IPSS y el componente de la vida
eficacia similar al observado en otros estudios con sabal
sexual del Urolife HPB QoL-9 (ρ de Pearson = -0,365, p =
en comparación con placebo. Un análisis de siete estudios
0,002), lo que indica que una menor incidencia de proble-
clínicos con un extracto lipofílico de sabal describe la ob-
mas urinarios se asocia con una mejor evaluación de la
servación de un total de 2.555 pacientes con una duración
función sexual. Además, hubo una alta correlación positiva
media de tratamiento de 300 días y un valor medio inicial
entre el bSFI y el componente de la vida sexual del Urolife
del IPSS de 14,72. Al final del tratamiento, el IPSS se re-
BHP QoL-9, lo que pone en evidencia que ambos cuestiona-
dujo en promedio un 31,2% (30). En otros dos estudios clí-
rios fueron válidos para la evaluación de las disfunciones
nicos se utilizó un extracto lipofílico de fruto de sabal (320
sexuales y, por consiguiente evidenciaron los cambios en
mg/díario) y, después de 6 meses, el IPSS se redujo en un
el mismo grado (ρ de Pearson = 0,607, p <0,0001).
26,3% (31) y el 37% (32), con reducciones en el grupo placebo
El análisis de los subgrupos confirmó estos hallazgos,
del 13,9% y 13,6% respectivamente.
mostrando que los pacientes con mayor afectación en el
En segundo lugar en el presente estudio se evaluó si el
momento de la inclusión (IPSS = 20-35) mostraron mejorías
tratamiento tenía una influencia positiva en las disfuncio-
superiores en los valores bSFI (p = 0,029) y en el compo-
nes sexuales concomitantes. En cuatro estudios clínicos
nente de la vida sexual del Urolife BPH QoL-9 (p = 0,032)
previos sobre el tratamiento de la HPB con preparados de
que los pacientes con menor sintomatología (IPSS = 8-19).
fruto de sabal también se habían evaluado las disfunciones
La comparación de los pacientes más jóvenes (menores de
sexuales como parámetro secundario, con resultados mix-
50 años) con los pacientes de mayor edad (51-80 años) no
tos. Sin embargo, en estos ensayos, los pacientes tenían
mostró una diferencia significativa respecto a los cambios
principalmente síntomas de HPB, sin presentar necesaria-
del IPSS, bSFI y el componente de la vida sexual del Urolife
mente disfunciones sexuales asociadas, por lo que se pue-
BPH QoL-9, ni tampoco tuvo influencia la administración de
de considerar que los datos obtenidos en estos ensayos
no son suficientes para demostrar de manera concluyente si el sabal tuvo una influencia positiva en las disfunciones
sexuales asociadas a la HPB. Willetts et al. (33), utilizando
Cinco pacientes reportaron seis reacciones adversas inclu-
el Índice Internacional de Función Eréctil (IIEF), observa-
yendo náuseas, eructos y regurgitación ácida, todos fueron
ron una tendencia de mejoría, con un aumento de 51,5 a
de naturaleza leve y se consideraron relacionadas con la
55,1 después de 12 semanas de tratamiento con sabal, en
medicación del estudio y dos casos de un ataque isquémi-
comparación con una pequeña disminución de 49,4 a 48,7
co transitorio en el mismo paciente y un prurito leve, que
con placebo. Sinescu et al. (34) informaron de una mejoría
no fueron relacionados con la medicación del estudio. De
significativa del IIEF de 44,4 a 50,8 después de 24 meses
un total de 82 pacientes, los datos de seis pacientes estu-
de tratamiento. En el ensayo realizado por Gerber et al.
vieron ausentes en la evaluación de la seguridad, del resto
(31), los pacientes rellenaron un cuestionario no específico
de los pacientes, el 89,5%, calificó la tolerabilidad como
sobre la función sexual, los resultados no indicaron nin-
muy buena y un 6,6% como buena. Del mismo modo, los
gún cambio ni el grupo placebo ni en el grupo tratado con
investigadores consideraron la tolerabilidad en el 90,8%
sabal. En un ensayo abierto, Bauer et al. (32) preguntaron a
de los casos como muy buena y el 5,3% como buena.
los pacientes si el tratamiento tuvo una influencia en su actividad sexual, las respuestas indicaron que la mayoría
Discusión
se mantuvo sin cambios, con dos pacientes que informaron
Este estudio piloto se diseñó para averiguar si un preparado
de un incremento.
de fruto de sabal tenía efecto sobre los síntomas del tracto
Para determinar si el sabal tenía una influencia positiva
urinario inferior y las disfunciones sexuales en pacien tes
en la disfunción sexual, fue importante confirmar que en
el momento de la inclusión todos los pacientes tuvieran
En primer lugar, se evaluó la mejoría de los síntomas urina-
disfunciones sexuales, lo que se confirmó con los valores
rios de la HPB mediante el cuestionario IPSS, considerado
iniciales del bSFI y del componente de la vida sexual del
el instrumento estándar para medir la severidad de los sín-
Urolife BPH QoL-9. O'Leary et al. (35) habían observado una
tomas (29). Se observó una reducción superior al 50%, lo que
puntuación media total de 27,7 del bSFI en una población
indica una buena respuesta al tratamiento, con un rango de
de 1.883 varones mayores de 50 años en Estados Unidos,
Cita Publicaciones
Revista de Fitoterapia 2012; 12 (2): 119-133
mientras que en el presente estudio, el mismo grupo de
datos experimentales también indican que la óxido nítrico
edad, tuvo un valor inicial menor de 20,1. En otro estudio,
sintasa (NOS) y el óxido nítrico (NO) podrían desempeñar
los pacientes con edades de 36,9 ± 12,0 años tenían un
un papel importante en el tejido de la uretra, los cuerpos
bSFI total promedio de 33,5 ± 2,2 (36) en comparación con
cavernosos, la próstata, los vasos deferentes y el cuello
el bSFI total inicial de 26,3 ± 6,6 observado en los pacien-
de la vejiga (39). Concentraciones reducidas de NOS / NO
tes del presente estudio con una edad entre 21 y 50 años.
en la próstata y la vejiga aumentan el tono del músculo
En un gran estudio de 2.829 pacientes con síntomas del
liso y pueden aumentar la proliferación de las células de
tracto urinario inferior (STUI), con una edad media de 65,9
la próstata (40), lo que indica que los inhibidores de la PDE-
años, se evaluaron las puntuaciones del componenente de
5 que aumentan la concentración de NO, pueden tener
la vida sexual del Urolife BPH QoL-9 y se observó un valor
efecto positivo sobre los STUI. Estudios clínicos iniciales
inicial total de 8,8 ± 0,1 (escala 0-30) (37), mientras que en
se han llevado a cabo con bloqueadores α-adrenérgicos e
el presente estudio se partió de una puntuación inicial de
inhibidores de las fosfodiesterasa-5 (PDE-5) (41). Los datos
130,0 ± 47,0 (escala de 0 a 300) en el grupo de pacientes
clínicos con bloqueadores α-adrenérgicos han demostra-
de 51 a 80 años.
do un buen efecto en el tratamiento de los síntomas de la
El presente estudio mostró un efecto significativo del sa-
HPB, pero con sólo una pequeña influencia positiva en las
bal sobre las disfunciones sexuales: el bSFI mejoró en un
disfunciones sexuales. En un estudio clínico en pacientes
40,2% y el componente de la vida sexual del Urolife QoL-9
con síntomas moderados a graves de HPB que tomaron 10
en un 42,0%. En cuanto a los resultados parciales sobre
mg/día de alfuzosina durante 6 meses, el IPSS disminuyó
los parámetros deseo sexual y función eréctil, también se
de 18,93 a 9,59 puntos, y el Cuestionario de Salud Sexual
observó mejoría, de un 35,3% y 37% respectivamente en
en el Hombre (MSHQ), en la subescala de la eyaculación,
el bSFI y un 35,7% y 44,9% en el componente de la vida
mejoró de 23,09 a 21,54, lo que fue estadísticamente signi-
sexual del Urolife QoL-9. La principal diferencia entre estas
ficativo, pero la relevancia clínica sigue siendo dudosa, con
dos escalas es la mayor ponderación del resultado parcial
una mejoría de aproximadamente sólo el 7%. El número total de los pacientes con disfunción eréctil moderada a
de la evaluación de problemas del bSFI. Se ha demostrado
severa se redujo de 35% a 22% (42). Estos resultados no
que ambos cuestionarios son igualmente sensibles en la
fueron confirmados en otro estudio donde los pacientes
evaluación de las disfunciones sexuales, lo cual ha sido
con síntomas de HPB tomaron 10 mg/día de alfuzosina
confirmado también por el análisis de correlación. Curio-
durante 12 semanas. Los resultados de este estudio de-
samente, se observó que era casi imposible para los pa-
mostraron que el IPSS disminuyó significativamente desde
cientes completar el cuestionario del bSFI sin la ayuda del
17,92 hasta 12,07, pero la puntuación de la eyaculación
médico, mientras que el componente respecto a la vida se-
del MSHQ empeoró significativamente desde 24,9 hasta
xual del Urolife QoL-9 fue muy fácil para los pacientes, que
27,14, y la puntuación de la erección y la satisfacción no
lo pudieron hacer de manera autónoma. En resumen, este
varió significativamente (43). En un gran ensayo abierto con
estudio ha demostrado por primera vez que un tratamiento
839 pacientes que padecían de STUI causados por HPB y
con sabal en pacientes con HPB y disfunciones sexuales
que tomaron 10 mg/día de alfuzosina durante 2 años, el
influye positivamente sobre ambas sintomatologías.
IPSS inicial de 15,5 se redujo en 7 puntos, mientras que el
Los resultados de la eficacia de este estudio son de mayor
valor total inicial del bSFI de 21,5 mejoró sólo ligeramente
importancia cuando se consideran otras opciones dispo-
durante el período de tratamiento, por lo que los autores
nibles en el mercado para el tratamiento simultáneo de
concluyeron que el tratamiento "al menos no tiene ningún
los STUI y las disfunciones sexuales. En la actualidad se
efecto perjudicial sobre las disfunciones sexuales" (44). Otro
debate si los bloqueadores α-adrenérgicos o los inhibido-
ensayo clínico abierto con 10 mg/día de alfuzosina mostró,
res de la fosfodiesterasa (PDE) pueden ser beneficiosos
además de una mejoría significativa del IPSS después de
para tratar los síntomas de ambos trastornos. Los mode-
1 año de tratamiento, una mejoría significativa también en
los experimentales han demostrado que los antagonistas
la puntuación de las disfunciones sexuales del Cuestiona-
α1-adrenérgicos pueden mejorar la disfunción eréctil, in-
rio Danés de la Puntuación de los Síntomas de la Próstata
fluyendo en el equilibrio entre la contracción y relajación
(45), mientras que un estudio comparativo de tamsulosina
del músculo liso del cuerpo cavernoso, la relajación de
y solifenacina, solos o en combinación, en pacientes con
los cuales conduce a una erección (38). Por otro lado, los
STUI también mejoró el IPSS, pero no se observaron cam-
Cita Publicaciones
Revista de Fitoterapia 2012; 12 (2): 119-133
bios significativos en el IIEF (46). Las reducciones del IPSS de unos 6 a 7 puntos que se observan en estos estudios con bloqueadores α-adrenérgicos fueron similares a las obser-vadas en ensayos controlados con placebo (47-48), pero no fueron superiores a las mejorías en el IPSS observadas en el estudio objeto de esta publicación, que está en conso-nancia con los ensayos de Debruyne et al. (18) y Zlotta et al. (49), que mostraron reducciones similares del IPSS después del tratamiento con un preparado de fruto de sabal y con tamsulosina. La principal diferencia entre los resultados del estudio objeto de esta publicación y la de los estudios citados con los bloqueadores α-adrenérgicos, es que los pacientes tratados con extracto de fruto de sabal pueden experimentar una mejora en sus disfunciones sexuales, mientras que este efecto no se puede esperar con los me-dicamentos bloqueadores α-adrenérgicos.
También sigue siendo dudoso que los inhibidores de la PDE-5 sean un buen tratamiento para los síntomas del tracto urinario inferior y las disfunciones sexuales. Los da-tos clínicos de los inhibidores de la PDE-5 han mostrado una buena mejoría en la disfunción eréctil, pero un efecto pequeño sobre los síntomas de la HPB. McVary et al. (50) observaron una mejoría significativa en el IPSS al cabo de 12 semanas de tratamiento con 100 mg de sildenafilo, con un cambio del IPSS de -6,3 frente a -1,9 con el placebo, así como una mejoría significativa de la función eréctil del IIEF. A juicio de Roehrborn et al. (51), la aplicación de diferentes
FIGURA 7. Hoja de Sabal. Foto: S. Cañigueral.
dosis de tadalafilo ha demostrado que una dosis mayor se correlaciona con una mejoría mayor del IPSS de +3,9
disfunción eréctil, los resultados del presente estudio son
con 2,5 mg y +5,2 con 20 mg, y la dosis de 5 mg mostró
al menos comparables con las de vardenafilo.
la mejor relación beneficio/riesgo. Después del período
Una solución que ha sido discutida en la literatura para
de tratamiento de 12 semanas, se observó también una
la reducción concomitante de los síntomas de la HPB y
mejoría en la función eréctil en el IIEF. Vardenafilo (20 mg)
la disfunción eréctil es la combinación de un bloqueador
tomado dos veces al día durante 8 semanas mejoró el IPSS
α-adrenérgico y un inhibidor de la PDE-5. Un pequeño es-
en 5,9 puntos, en comparación con 3,6 puntos del placebo,
tudio investigó la alfuzosina, el sildenafilo o la combinación
se observaron cambios significativos también en la disfun-
de ambos en los STUI y en la disfunción eréctil. Después de
ción eréctil del IIEF y en el componente de la vida sexual
12 semanas de tratamiento, los valores iniciales del IPSS,
del Urolife QoL-9, que mejoró en un 62,6% en comparación
que eran entre 16,9 y 17,8, se redujeron significativamente
con un 17,2% del placebo (52). A pesar que el IPSS mejoró
en todos los grupos de tratamiento, con la mayor reducción
en estos ensayos, curiosamente, no se reportaron cambios
(24,1%) en el grupo de la combinación. La puntuación de
en la flujometría. En resumen, el presente estudio clínico
la función eréctil del IIEF fue significativamente mejorada
muestra una mejoría en los STUI mayor que la observada
mediante el sildenafilo y la combinación sildenafilo-alfu-
en los estudios con inhibidores de la PDE-5, y con mejores
zosina, pero no en el grupo al que se le administró solo
efectos en la disfunción eréctil. Si consideramos el com-
alfuzosina (53). Otro ensayo de combinación de sildenafilo o
ponente sobre la vida sexual del Urolife QoL-9, que evalúa
tamsulosina mostró resultados similares, con una mejoría
un amplio espectro de disfunciones sexuales, y no solo la
del IPSS mayor con la combinación (-40,1%), seguida de
Cita Publicaciones
Revista de Fitoterapia 2012; 12 (2): 119-133
tamsulosina (-36,2%) y sildenafilo (-28,2%); el IIEF mejo-
estudio epidemiológico llevado a cabo con urólogos y mé-
ró significativamente con el sildenafilo y la combinación,
dicos de medicina interna en Estados Unidos, se estima
pero no con tamsulosina (54). En otro ensayo, se añadieron
que 18-27% de los pacientes que toman un medicamento
100 mg de udenafilo a una terapia estable con bloqueador
bloqueador α-adrenérgico sufren de trastornos de la eya-
α-adrenérgico en pacientes con HPB y disfunción eréctil
culación y el 16-22% de los hombres que toman un inhi-
durante 8 semanas. El IPSS se redujo en 2,8 puntos, y el
bidor de la 5α-reductasa sufren de disfunción eréctil (60).
IIEF-5 mejoró en más de 5 puntos, lo que indica que una
Sin embargo, en la última guía de la Asociación Americana
combinación o un complemento en la terapia de udenafilo
de Urología para el tratamiento de los síntomas de HPB,
puede ser beneficiosa. (55). Comparando estos datos con
también se aboga por utilizar una combinación de bloquea-
los resultados del presente estudio, con una reducción
dores α-adrenérgicos e inhibidores de la 5α-reductasa (61),
del IPSS del 51% y con una mejoría de las disfunciones
un protocolo diseñado para lograr una mejor eficacia, pero
sexuales en un 40,1%, medidos con el bSFI, el tratamien-
sin examinar a fondo los efectos secundarios adicionales
to con extracto de fruto de sabal arrojó unos resultados
de estos dos medicamentos como se muestra en ensayos
de eficacia similares a la combinación de un bloqueador
de la combinación (39).
α-adrenérgico y un inhibidor de la PDE-5.
El presente ensayo tiene algunas limitaciones, ya que fue
Los inhibidores de la fosfodiesterasa-5 son tratamientos
diseñado como un estudio piloto no controlado para diluci-
costosos, por lo que se hace necesario realizar una eva-
dar si se observaba algún efecto en un tratamiento a base
luación costo-beneficio para una prescripción extensiva
de fruto de sabal. En consecuencia, el tamaño del efecto
de inhibidores de la PDE-5. En los EUA, una sola dosis de
placebo sólo puede ser estimativo. Por otra parte, hubo un
25 mg de sildenafilo cuesta unas ocho veces más que un
fuerte efecto "centro dependiente", ya que un centro reclu-
agente bloqueador α-adrenérgico como doxazosina 1 mg
tó sustancialmente más pacientes que los otros. El análisis
(56) o 30 veces más que 0,4 mg de tamsulosina en Alemania
de los subgrupos no revela diferencias significativas en
(57), mientras que el costo de una dosis diaria de Prostasan®
las características de los pacientes entre los centros, sin
está en el rango inferior de un bloqueador α-adrenérgico.
embargo, estos análisis estaban limitados por el escaso
Esta diferencia de precios, junto con su eficacia sólo mo-
número de pacientes en los otros cinco centros en su con-
derada, hacen dudar si los inhibidores de la PDE-5 deben
junto. Para confirmar los hallazgos del presente estudio,
ser utilizados como tratamiento estándar para los síntomas
el siguiente paso sería hacer un estudio clínico controlado
con placebo y con una distribución más equilibrada de los
Al examinar la seguridad y la tolerabilidad, los datos del
pacientes en los diversos centros.
presente estudio están en concordancia con resultados an-teriores, e indican que el extracto de fruto de sabal fue muy
bien tolerado, en contraste con los tratamientos estándar
Este es el primer estudio diseñado para demostrar que el
para los STUI. Un problema importante para los pacientes
tratamiento con extracto de fruto de sabal no sólo tiene
que tomaban un bloqueador α-adrenérgico y/o un inhibidor
una buena eficacia en la reducción de los síntomas de la
de la 5α-reductasa es la ocurrencia de reacciones adversas
HPB, sino también un efecto concomitante en las disfun-
en la esfera sexual, que son la causa por la cual muchos
ciones sexuales. El tratamiento con extracto de fruto de
hombres interrumpen el tratamiento (58). Los datos de los
sabal fue tan eficaz en la reducción de los síntomas de
estudios muestran que del 2 al 16% de todos los pacien-
la HPB como un bloqueador α-adrenérgico o un inhibidor
tes bajo tratamiento con inhibidores de la 5α-reductasa
de la 5α-reductasa, pero, a diferencia de estos, el fruto
experimentan disfunción eréctil, disminución de la libido
de sabal se asoció con una mejoría de las disfunciones
y disminución del volumen de la eyaculación (el doble de
sexuales evaluadas mediante el bSFI y el componente de
la frecuencia observada con placebo), mientras que los
la vida sexual del Urolife QoL-9. En comparación con los
bloqueadores α-adrenérgicos, en particular la tamsulosi-
inhibidores de la fosfodiesterasa, el tratamiento con fru-
na, se han relacionado con trastornos de la eyaculación en
to de sabal no tuvo la misma eficacia en la mejoría de la
alrededor del 10% de los pacientes (59).
disfunción eréctil, pero fue igualmente eficaz en el trata-
En la práctica diaria, la tasa de incidencia puede ser in-
miento de las disfunciones sexuales en general, con una
cluso mayor que en los estudios clínicos. En un amplio
mayor reducción del IPSS. El coste diario del tratamiento
Cita Publicaciones
Revista de Fitoterapia 2012; 12 (2): 119-133
con el extracto de fruto de sabal es mucho menor que el de
5. Gur S, Kadowitz PJ, Hellstrom WJ. Guide to drug therapy for
otros medicamentos, por ejemplo en Suiza, el costo sería
lower urinary tract symptoms in patients with benign prostatic
de 0,75 francos suizos para el medicamento a base de fruto
obstruction: implications for sexual dysfunction. Drugs 2008; 68
de sabal en comparación con 22,30 francos suizos para 100
(2): 209-229.
mg de sildenafilo (62).
6. Braun MH, Sommer F, Haupt G, Mathers MJ, Reifenrath B, Engelmann UH. Lower urinary tract symptoms and erectile dys-
En el presente estudio se observa la misma eficacia que con
function: co-morbidity or typical „Aging Male" symptoms? Results
la utilización combinada de bloqueadores α-adrenérgicos
of the „Cologne Male Survey". Eur Urol 2003; 44 (5): 588-594.
e inhibidores de la 5-fosfodiesterasa, pero el tratamiento
7. Rosen R, Altwein J, Boyle P, Kirby RS, Lukacs B, Meuleman E, et
con fruto de sabal presenta una tolerabilidad mucho me-
al. Lower urinary tract symptoms and male sexual dysfunction: the
jor. Basándose en estos prometedores resultados, que se
multinational survey of the aging male (MSAM-7). Eur Urol 2003;
reflejan también en la buena aceptación de los pacientes
44 (6): 637-649.
y los investigadores, consideramos el ectracto de fruto de
8. Rosen RC, Giuliano F, Carson CC. Sexual dysfunction and lower
sabal como el tratamiento de primera línea para pacien-
urinary tract symptoms (LUTS) associated with benign prostatic
tes con síntomas de HPB leve y moderada, ya que también
hyperplasia (BPH). Eur Urol 2005; 47 (6): 824-837.
puede mejorar las disfunciones sexuales concomitantes,
9. Novara G, Galfano A, Ficarra V, Artibani W. Anticholinergic drugs in patients with bladder outlet obstruction and lower uri-
teniendo una muy buena tolerabilidad y rentabilidad.
nary tract symptoms: A systematic review. Eur Urol 2006; 50 (4):
675-683.
10. Kaplan SA. AUA Guidelines and their impact on the manage-
Este artículo es una traducción adaptada del artículo: Suter
ment of BPH: An update. Rev Urol 2004; 6 (Suppl 9): S46-52.
A, Saller R, Riedi E, Heinrich M. Improving BPH symptoms
11. Dull P, Reagan RW Jr, Bahnson RR. Managing benign prostatic
and sexual dysfunctions with a saw palmetto preparation?
hyperplasia. Am Fam Physician 2002; 66 (1): 77-84.
Results from a pilot trial. Phytother Res 2012, cuya versión
12. Carbone DJ Jr, Hodges S. Medical therapy for benign prostatic
corregida se ha publicado online el 26/9/2012 en Wiley
hyperplasia: sexual dysfunction and impact on quality of life. Int J
Online Library, DOI: 10.1002/ptr.4696, http://onlinelibrary.
Impot Res 2003; 15 (4): 299-306.
13. Erdemir F, Harbin A, Hellstrom WJ. 5-alpha reductase inhibi-tors and erectile dysfunction: the connection. J Sex Med 2008; 5
(12): 2917-2924.
Nos gustaría dar las gracias a los siguientes investiga-
14. Naslund MJ, Miner M. A review of the clinical efficacy and
dores por su participación en este estudio: Daniel Borer
safety of 5alpha-reductase inhibitors for the enlarged prostate.
(Moerigen), Eva Ditrych (Berna), Simón Feldhaus (Brunnen),
Clin Ther 2007; 29 (1): 17-25.
Manfred Hoesle (Zurich), y Trinkler Félix (Zollikon).
15. Bennett BC HJ. Uses of saw palmetto (Serenoa repens, Areca-ceae) in Florida. Economic Botany 1998; 52: 381-393.
Conflicto de intereses
16. Ulbricht C, Basch E, Bent S, Boon H, Corrado M, Foppa I. Evi-
El estudio fue financiado por A. Vogel Bioforce AG, donde
dence-based systematic review of saw palmetto by the Natural
A. Suter trabaja en el departamento investigación médica.
Standard Research Collaboration. J Soc Integr Oncol 2006; 4 (4): 170-186.
17. Carraro JC, Raynaud JP, Koch G, Chisholm GD, Di Silverio F, Teillac P, et al. Comparison of phytotherapy (Permixon) with finas-
1. Dixon JS GJ. Macro-anatomy of the prostate. En: Kirby RS MJ,
teride in the treatment of benign prostate hyperplasia: a rando-
Fitzpatrick JM, Roehrborn CG, Boyle P (ed.) Textbook of benign
mized international study of 1098 patients. Prostate 1996; 29 (4):
prostatic hyperplasia. Oxon: Taylor & Francis: 2-10; 2005.
231-240; discussion 241-232.
2. Isaacs JT, Coffey DS. Etiology and disease process of benign
18. Debruyne F, Boyle P, Calais Da Silva F, Gillenwater JG, Hamdy
prostatic hyperplasia. Prostate 1989; Suppl 2: 33-50.
FC, et al. Evaluation of the clinical benefit of permixon and tam-
3. McVary KT. BPH: epidemiology and comorbidities. Am J Manag
sulosin in severe BPH patients-PERMAL study subset analysis. Eur
Care 2006; 12 (Suppl 5): S122-128.
Urol 2004; 45 (6): 773-779; discussion 779-780.
4. Berry SJ, Coffey DS, Walsh PC, Ewing LL. The development of
19. Wilt T, Ishani A, Mac Donald R. Serenoa repens for benign
human benign prostatic hyperplasia with age. J Urol 1984; 132
prostatic hyperplasia. Cochrane Database Syst Rev CD001423;
(3): 474-479.
Cita Publicaciones
Revista de Fitoterapia 2012; 12 (2): 119-133
20. Habib FK, Ross M, Ho CK, Lyons V, Chapman K. Serenoa repens
33. Willetts KE, Clements MS, Champion S, Ehsman S, Eden JA.
(Permixon) inhibits the 5alpha-reductase activity of human prosta-
Serenoa repens extract for benign prostate hyperplasia: a rando-
te cancer cell lines without interfering with PSA expression. Int J
mized controlled trial. BJU Int 2003; 92 (3): 267-270.
Cancer 2005; 114 (2): 190-194.
34. Sinescu I, Geavlete P, Multescu R, Gangu C, Miclea F, Coman I,
21. Abe M, Ito Y, Oyunzul L, Oki-Fujino T, Yamada S. Pharmacologi-
et al. Long-term efficacy of Serenoa repens treatment in patients
cally relevant receptor binding characteristics and 5alpha-reducta-
with mild and moderate symptomatic benign prostatic hyperpla-
se inhibitory activity of free Fatty acids contained in saw palmetto
sia. Urol Int 2011; 86 (3): 284-289.
extract. Biol Pharm Bull 2009; 32 (4): 646-650.
35. O‘Leary MP, Rhodes T, Girman CJ, Jacobson DJ, Roberts RO,
22. Breu W, Hagenlocher M, Redl K, Tittel G, Stadler F, Wagner
Lieber MM, et al. Distribution of the Brief Male Sexual Inventory in
H. Anti-inflammatory activity of sabal fruit extracts prepared with
community men. Int J Impot Res 2003; 15 (3): 185-191.
supercritical carbon dioxide. In vitro antagonists of cyclooxygena-
36. Collins S, Upshaw J, Rutchik S, Ohannessian C, Ortenberg J,
se and 5-lipoxygenase metabolism. Arzneimittelforschung 1992;
Albertsen P. Effects of circumcision on male sexual function: de-
42 (4): 547-551.
bunking a myth? J Urol 2002; 167 (5): 2111-2112.
23. Iglesias-Gato D, Carsten T, Vesterlund M, Pousette A, Schoop
37. Lukacs B, Comet D, Grange JC, Thibault P. Construction and
R, Norstedt G. Androgen-independent Effects of Serenoa repens
validation of a short-form benign prostatic hypertrophy health-re-
Extract (Prostasan) on Prostatic Epithelial Cell Proliferation and
lated quality-of-life questionnaire. BPH Group in General Practice.
Inflammation. Phytother Res 2011; 26 (2); 259-264. DOI: 10.1002/
Br J Urol 1997; 80 (5): 722-730.
38. Hellstrom WJ, Kendirci M. Type 5 phosphodiesterase inhibi-
24. Suzuki M, Oki T, Sugiyama T, Umegaki K, Uchida S, Yamada
tors: curing erectile dysfunction. Eur Urol 2006; 49 (6): 942-945.
S. Muscarinic and alpha 1-adrenergic receptor binding characte-
39. Ehren I, Adolfsson J, Wiklund NP. Nitric oxide synthase activity
ristics of saw palmetto extract in rat lower urinary tract. Urology
in the human urogenital tract. Urol Res 1994; 22 (5): 287-290.
2007; 69 (6): 1216-1220.
40. Mirone V, Sessa A, Giuliano F, Berges R, Kirby M, Moncada I.
25. Skolarus TA, Wei JT. Measurement of benign prostatic hyper-
Current benign prostatic hyperplasia treatment: impact on sexual
plasia treatment effects on male sexual function. Int J Impot Res
function and management of related sexual adverse events. Int J
2009; 21 (5): 267-274.
Clin Pract 2011; 65 (9): 1005-1013.
26. O‘Leary MP, Fowler FJ, Lenderking WR, Barber B, Sagnier PP,
41. Kaminetsky J. Comorbid LUTS and erectile dysfunction: opti-
Guess HA, et al. A brief male sexual function inventory for urology.
mizing their management. Curr Med Res Opin 2006; 22 (12): 2497-
Urology 1995; 46 (5): 697-706.
27. Lukacs B, Grange JC, Comet D. One-year follow-up of 2829
42. Leungwattanakij S, Watanachote D, Noppakulsatit P, Petchpai-
patients with moderate to severe lower urinary tract symptoms
buol T, Choeypunt N, Tongbai T, et al. Sexuality and management
treated with alfuzosin in general practice according to IPSS and a
of benign prostatic hyperplasia with alfuzosin: SAMBA Thailand. J
health-related quality-of-life questionnaire. BPM Group in General
Sex Med 2010; 7 (9): 3115-3126.
Practice. Urology 2000; 55 (4): 540-546.
43. Kim MK, Cheon J, Lee KS, Chung MK, Lee JY, Lee SW, et al. An
28. Sádaba B, Fernández V, Honorato J. Metodología y tipos de en-
open, non-comparative, multicentre study on the impact of alfuzo-
sayos clínicos con medicamentos. En: Zubiri F , Honorato J. Curso
sin on sexual function using the Male Sexual Health Questionnaire
de Farmacología clínica aplicada. El Médico Formación Acreditada
in patients with benign prostate hyperplasia. Int J Clin Pract 2010;
online; 2011. Disponible en: http://2011.elmedicointeractivo.com/
64 (3): 345-350.
44. Elhilali M, Emberton M, Matzkin H, van Moorselaar RJ, Har-
29. Simpson RJ. Benign prostatic hyperplasia. Br J Gen Pract 1997;
tung R, Harving N, et al. Long-term efficacy and safety of alfuzosin
47 (417): 235-240.
10 mg once daily: a 2-year experience in ‚real-life‘ practice. BJU
30. Boyle P, Robertson C, Lowe F, Roehrborn C. Updated meta-
Int 2006; 97 (3): 513-519.
analysis of clinical trials of Serenoa repens extract in the
45. van Moorselaar RJ, Hartung R, Emberton M, Harving N, Matz-
treatment of symptomatic benign prostatic hyperplasia. BJU Int
kin H, Elhilali M, et al. Alfuzosin 10 mg once daily improves sexual
2004; 93 (6): 751-756.
function in men with lower urinary tract symptoms and concomi-
31. Gerber GS, Kuznetsov D, Johnson BC, Burstein JD. Randomi-
tant sexual dysfunction. BJU Int 2005; 95 (4): 603-608.
zed, double-blind, placebo-controlled trial of saw palmetto in men
46. Seo DH, Kam SC, Hyun JS. Impact of lower urinary tract symp-
with lower urinary tract symptoms. Urology 2001; 58 (6): 960-964;
toms/benign prostatic hyperplasia treatment with tamsulosin and
discussion 964-965.
solifenacin combination therapy on erectile function. Korean J
32. Bauer HW, Casarosa C, Cosci M, Fratta M, Blessmann G. Saw
Urol 2011; 52 (1): 49-54.
palmetto fruit extract for treatment of benign prostatic hyperpla-
47. van Kerrebroeck P, Jardin A, Laval KU, van Cangh P. Efficacy
sia. Results of a placebo-controlled double-blind study. MMW
and safety of a new prolonged release formulation of alfuzosin 10
Fortschr Med 1999; 141 (25): 62.
mg once daily versus alfuzosin 2.5 mg thrice daily and placebo in
Cita Publicaciones
Revista de Fitoterapia 2012; 12 (2): 119-133
patients with symptomatic benign prostatic hyperplasia. ALFORTI
54. Tuncel A, Nalcacioglu V, Ener K, Aslan Y, Aydin O, Atan A.
Study Group. Eur Urol 2000; 37 (3): 306-313.
Sildenafil citrate and tamsulosin combination is not superior to
48. Nordling J. Efficacy and safety of two doses (10 and 15 mg) of
monotherapy in treating lower urinary tract symptoms and erectile
alfuzosin or tamsulosin (0.4 mg) once daily for treating symptoma-
dysfunction. World J Urol 2010; 28 (1): 17-22.
tic benign prostatic hyperplasia. BJU Int 95 (7): 1006-1012.
55. Chung BH, Lee JY, Lee SH, Yoo SJ, Lee SW, Oh CY. Safety
and efficacy of the simultaneous administration of udenafil and an
49. Zlotta AR, Teillac P, Raynaud JP, Schulman CC. Evaluation of
alpha-blocker in men with erectile dysfunction concomitant with
male sexual function in patients with Lower Urinary Tract Symp-
BPH/LUTS. Int J Impot Res 21 (2): 122-128.
toms (LUTS) associated with Benign Prostatic Hyperplasia (BPH) treated with a phytotherapeutic agent (Permixon), Tamsulosin or
56. Stafford RS, Radley DC. The potential of pill splitting to achie-
Finasteride. Eur Urol 2005; 48 (2): 269-276.
ve cost savings. Am J Manag Care 2002; 8 (8): 706-712.
57. Schneider D, Richling F. Checkliste Arzneimittel. Georg Thieme
50. McVary KT, Monnig W, Camps JL, Jr., Young JM, Tseng LJ,
Verlag: Stuttgart; 2008.
van den Ende G. Sildenafil citrate improves erectile function and urinary symptoms in men with erectile dysfunction and lower uri-
58. Roehrborn CG. Lower urinary tract symptoms, benign prostatic
nary tract symptoms associated with benign prostatic hyperplasia:
hyperplasia, erectile dysfunction, and phosphodiesterase-5 inhibi-
tors. Rev Urol 2004; 6 (3): 121-127.
a randomized, double-blind trial. J Urol 2007; 177 (3): 1071-1077.
59. Gacci M, Eardley I, Giuliano F, Hatzichristou D, Kaplan SA, Ma-
51. Roehrborn CG, McVary KT, Elion-Mboussa A, Viktrup L. Ta-
ggi M, et al. Critical analysis of the relationship between sexual
dalafil administered once daily for lower urinary tract symptoms
dysfunctions and lower urinary tract symptoms due to benign pros-
secondary to benign prostatic hyperplasia: a dose finding study. J
tatic hyperplasia. Eur Urol 2011; 60 (4): 809-825.
Urol 2008; 180 (4): 1228-1234.
60. Seftel A, Rosen R, Kuritzky L. Physician perceptions of sexual
52. Stief CG, Porst H, Neuser D, Beneke M, Ulbrich E. A rando-
dysfunction related to benign prostatic hyperplasia (BPH) symp-
mised, placebo-controlled study to assess the efficacy of twice-
toms and sexual side effects related to BPH medications. Int J
daily vardenafil in the treatment of lower urinary tract symptoms
Impot Res 2007; 19 (4): 386-392.
secondary to benign prostatic hyperplasia. Eur Urol 2008; 53 (6):
61. McVary KT, Roehrborn CG, Avins AL, Barry MJ, Bruskewitz RC,
Donnell RF, Foster HE, et al. Update on AUA guideline on the ma-
53. Kaplan SA, Gonzalez RR, Te AE. Combination of Alfuzosin and
nagement of benign prostatic hyperplasia. J Urol 2011; 185 (5):
sildenafil is superior to monotherapy in treating lower urinary
tract symptoms and erectile dysfunction. Eur Urol 2007; 51 (6):
62. Stebler T. Viagra (Sildenafil). http://www.engelapo.ch/medis/
viagra.htm; 2009. Accessed at 12 November 2011.
Cita Publicaciones
A Publicaciones y Documentación, S.L.
CITA Publicaciones y Documentación, S.L.
46240 Carlet (Valencia) · España
46240 Carlet (Valencia) · España
Tel.: 96 299 32 39
Tel.: 96 299 32 39
[email protected]
Cita Publicaciones
Foto: S. Foster
Source: http://www.tu-salud.net/archivos/201508/separata_sabal_rdf_12_2.pdf?1
A Research Brief is a brief summary of research Research Brief findings. Context Matters When Segmenting THE PROBLEM Market segmentation is a process that can help managers identify and target those con-sumers with whom they can achieve a competitive advantage. This process can be based on consumer variables but may not always effectively account for different situations (i.e. contexts). Segmentation that incorporates context-dependent preferences promises to deliver richer insights, but can be quite chal enging. For example, if asked in the middle of the
Univ. Sci. 2014, Vol. 19 (1): 11-29 Freely available on line Técnicas analíticas contemporáneas para la identificación de residuos de sulfonamidas, quinolonas y cloranfenicol Y. Verónica Talero-Pérez scar Julio Medina 1, Wilson Rozo-Núñez2 Contemporary analytical techniques to identify residues of sulfonamides,

